| PRMT1 |
|---|
 |
| Ідентифікатори |
|---|
| Символи | PRMT1, ANM1, HCP1, HRMT1L2, IR1B4, protein arginine methyltransferase 1 |
|---|
| Зовнішні ІД | OMIM: 602950 MGI: 107846 HomoloGene: 21477 GeneCards: PRMT1 |
|---|
| шифр КФ | 2.1.1.321 |
|---|
| Онтологія гена |
|---|
| Молекулярна функція | • GO:0102674, GO:0102675 methyltransferase activity
• histone methyltransferase activity
• transferase activity
• histone methyltransferase activity (H4-R3 specific)
• methyl-CpG binding
• mitogen-activated protein kinase p38 binding
• GO:0001948, GO:0016582 protein binding
• identical protein binding
• enzyme binding
• N-methyltransferase activity
• protein-arginine omega-N asymmetric methyltransferase activity
• RNA binding
• protein methyltransferase activity
• protein-arginine N-methyltransferase activity
• histone-arginine N-methyltransferase activity
• GO:0016275 protein-arginine omega-N monomethyltransferase activity
• S-adenosyl-L-methionine binding
|
|---|
| Клітинна компонента | • цитоплазма
• нуклеоплазма
• methylosome
• клітинне ядро
• гіалоплазма
|
|---|
| Біологічний процес | • positive regulation of p38MAPK cascade
• positive regulation of hemoglobin biosynthetic process
• histone H4-R3 methylation
• positive regulation of erythrocyte differentiation
• negative regulation of megakaryocyte differentiation
• cell surface receptor signaling pathway
• Метилювання
• peptidyl-arginine methylation
• histone methylation
• neuron projection development
• peptidyl-arginine N-methylation
• peptidyl-arginine methylation, to asymmetrical-dimethyl arginine
• DNA damage response, signal transduction by p53 class mediator resulting in cell cycle arrest
• GO:0009373 regulation of transcription, DNA-templated
• Метилювання білків
• positive regulation of cell population proliferation
• regulation of megakaryocyte differentiation
• in utero embryonic development
• histone arginine methylation
• protein homooligomerization
|
|---|
| Джерела:Amigo / QuickGO | |
| Шаблон експресії |
|---|
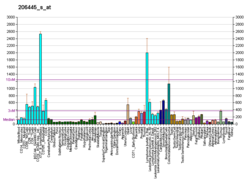 |
| Більше даних |
| Ортологи |
|---|
| Види | Людина | Миша |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (мРНК) | | NM_001207042
NM_001536
NM_198318
NM_198319 |
| | NM_001252476
NM_001252477
NM_019830 |
|
|---|
| RefSeq (білок) | | NP_001193971
NP_001527
NP_938074 |
| | NP_001239405
NP_001239406
NP_062804 |
|
|---|
| Локус (UCSC) | Хр. 19: 49.68 – 49.69 Mb | Хр. 7: 44.63 – 44.64 Mb |
|---|
| PubMed search | [1] | [2] |
|---|
| Вікідані |
| Див./Ред. для людей | Див./Ред. для мишей |
|
PRMT1 (англ. Protein arginine methyltransferase 1) – білок, який кодується однойменним геном, розташованим у людей на короткому плечі 19-ї хромосоми.[3] Довжина поліпептидного ланцюга білка становить 361 амінокислот, а молекулярна маса — 41 516[4].
Послідовність амінокислот
| 10 | | 20 | | 30 | | 40 | | 50 |
|---|
| MENFVATLAN | | GMSLQPPLEE | | VSCGQAESSE | | KPNAEDMTSK | | DYYFDSYAHF |
| GIHEEMLKDE | | VRTLTYRNSM | | FHNRHLFKDK | | VVLDVGSGTG | | ILCMFAAKAG |
| ARKVIGIECS | | SISDYAVKIV | | KANKLDHVVT | | IIKGKVEEVE | | LPVEKVDIII |
| SEWMGYCLFY | | ESMLNTVLYA | | RDKWLAPDGL | | IFPDRATLYV | | TAIEDRQYKD |
| YKIHWWENVY | | GFDMSCIKDV | | AIKEPLVDVV | | DPKQLVTNAC | | LIKEVDIYTV |
| KVEDLTFTSP | | FCLQVKRNDY | | VHALVAYFNI | | EFTRCHKRTG | | FSTSPESPYT |
| HWKQTVFYME | | DYLTVKTGEE | | IFGTIGMRPN | | AKNNRDLDFT | | IDLDFKGQLC |
| ELSCSTDYRM | | R |
Кодований геном білок за функціями належить до трансфераз, метилтрансфераз, фосфопротеїнів. Задіяний у такому біологічному процесі, як альтернативний сплайсинг. Білок має сайт для зв'язування з S-аденозил-L-метіоніном. Локалізований у цитоплазмі, ядрі.
Література
- Nikawa J., Nakano H., Ohi N. (1996). Structural and functional conservation of human and yeast HCP1 genes which can suppress the growth defect of the Saccharomyces cerevisiae ire15 mutant. Gene. 171: 107—111. PMID 8675017 DOI:10.1016/0378-1119(96)00073-X
- Scorilas A., Black M.H., Talieri M., Diamandis E.P. (2000). Genomic organization, physical mapping, and expression analysis of the human protein arginine methyltransferase 1 gene. Biochem. Biophys. Res. Commun. 278: 349—359. PMID 11097842 DOI:10.1006/bbrc.2000.3807
- The status, quality, and expansion of the NIH full-length cDNA project: the Mammalian Gene Collection (MGC). Genome Res. 14: 2121—2127. 2004. PMID 15489334 DOI:10.1101/gr.2596504
- Tang J., Kao P.N., Herschman H.R. (2000). Protein-arginine methyltransferase I, the predominant protein-arginine methyltransferase in cells, interacts with and is regulated by interleukin enhancer-binding factor 3. J. Biol. Chem. 275: 19866—19876. PMID 10749851 DOI:10.1074/jbc.M000023200
- Miyata S., Mori Y., Tohyama M. (2008). PRMT1 and Btg2 regulates neurite outgrowth of Neuro2a cells. Neurosci. Lett. 445: 162—165. PMID 18773938 DOI:10.1016/j.neulet.2008.08.065
- Pahlich S., Zakaryan R.P., Gehring H. (2008). Identification of proteins interacting with protein arginine methyltransferase 8: the Ewing sarcoma (EWS) protein binds independent of its methylation state. Proteins. 72: 1125—1137. PMID 18320585 DOI:10.1002/prot.22004
Примітки
- ↑ Human PubMed Reference:.
- ↑ Mouse PubMed Reference:.
- ↑ HUGO Gene Nomenclature Commitee, HGNC:5187 (англ.) . Архів оригіналу за 22 березня 2016. Процитовано 12 вересня 2017.
- ↑ UniProt, Q99873 (англ.) . Архів оригіналу за 24 липня 2017. Процитовано 12 вересня 2017.
Див. також
 | Це незавершена стаття про білки.
Ви можете допомогти проєкту, виправивши або дописавши її. |
 Портал «Біологія» Портал «Біологія»  Портал «Хімія» Портал «Хімія»
|










