| MB |
|---|
 |
| Structuri disponibile |
|---|
| PDB | Căutare Ortholog: PDBe RCSB |
|---|
| Coduri de identificare în PDB |
|---|
3RGK |
|
|
| Identificatori |
|---|
| Alias | MB |
|---|
| Identificări externe | OMIM: 160000 MGI: 96922 HomoloGene: 3916 GeneCards: MB |
|---|
| Localizarea genei (om) |
|---|
 | | Cro. | Cromozomul uman 22[1] |
|---|
| | Bandă | 22q12.3 | Start | 35,606,764 pb[1] |
|---|
| Final | 35,637,951 pb[1] |
|---|
|
| Modelul de exprimare ARN |
|---|
 | | Mai multe date de referință pentru exprimare |
|
| Ontologia genei |
|---|
| Funcția moleculară | • oxygen binding
• heme binding
• metal ion binding
• oxygen carrier activity
|
|---|
| Componenta celulară | • exozom extracelular
• citosol
|
|---|
| Procesul biologic | • response to hormone
• heart development
• slow-twitch skeletal muscle fiber contraction
• răspuns la hipoxie
• enucleate erythrocyte differentiation
• response to hydrogen peroxide
• brown fat cell differentiation
• oxygen transport
• GO:0015915 transport
|
|---|
| Surse: Amigo / QuickGO |
|
| Ortologi |
|---|
| Specie | Om | Șoarece |
|---|
| Entrez | | |
|---|
| Ensembl | | |
|---|
| UniProt | | |
|---|
| RefSeq (mRNA) | |
|---|
NM_005368
NM_203377
NM_203378
NM_001362846 |
| |
|---|
NM_001164047
NM_001164048
NM_013593 |
|
|---|
| RefSeq (proteine) | NP_005359
NP_976311
NP_976312
NP_001349775
NP_001369738
|
|---|
NP_001369739
NP_001369740
NP_001369741
NP_001369742 |
| |
|---|
NP_001157519
NP_001157520
NP_038621 |
|
|---|
| Localizare (UCSC) | Chr 22: 35.61 – 35.64 Mb | n/a |
|---|
| Căutare PubMed | [2] | [3] |
|---|
| Wikidata |
| Vedeți/Editați Om | Vedeți/Editați Șoarece |
|
Mioglobina (abreviat Mb) este o proteină prezentă în fibrele musculare scheletice și cardiace, cu rol în legarea oxigenului. Aceasta este prezentă la majoritatea vertebratelor și la aproape toate mamiferele. Mioglobina poate fi găsită în sânge doar atunci când aceasta este eliberată în urma unei leziuni musculare.
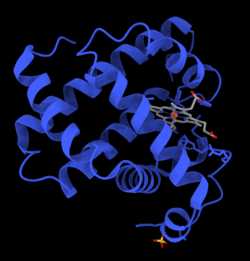
Mioglobina este o proteină globulară formată dintr-un singur lanț de 154 de aminoacizi, conținând o grupare hem înfășurat de o apoproteină. Este format din opt alfa-helixuri și un miez hidrofob. Are o greutate moleculară de 16700 daltoni, și este cel mai important pigment care transportă oxigen din țesuturile musculare. Spre deosebire de hemoglobina din sânge, mioglobina nu se leagă cooperativ de oxigen, legarea oxigenului de mioglobină nefiind afectată deci de presiunea oxigenului în țesuturile înconjurătoare. Concentrațiile mari de mioglobină din celulele musculare permit organismelor să țină respirația un timp mai îndelungat. Mamiferele marine, cum ar fi balenele și focile, prezintă o concentrație crescută de mioglobină în mușchi.
Mioglobina a fost prima proteină a cărei structură tri-dimensională a fost dezvăluită. În 1958, John Kendrew și asociații au determinat cu succes structura mioglobinei folosind cristalografie cu raze X de înaltă rezoluție. Pentru această descoperire, John Kendrew a primit în 1962 Premiul Nobel pentru Chimie împreună cu Max Perutz. În ciuda faptului că este una din cele mai studiate proteine în biologie, funcția propriu-zisă fiziologică nu a fost încă definitiv stabilită: șoarecii modificați genetic astfel încât să nu prezinte mioglobină sunt viabili, dar au arătat o reducere de 30% a funcției sistolice. Ei s-au adaptat la acest deficit prin mecanism hipoxic și vasodilatație crescută.
Vezi și
Bibliografie
Legături externe
- ^ a b c GRCh38: Ensembl ediția 89: ENSG00000198125 - Ensembl, mai 2017
- ^ „Referința PubMed pentru om:”.
- ^ „Referința PubMed pentru șoarece:”.


















 Mioglobină
Mioglobină