Pentafluoreto de iodo
| Pentafluoreto de iodo Alerta sobre risco à saúde | |
|---|---|
 |  |
| Outros nomes | Fluoreto iódico |
| Identificadores | |
| Número CAS | 7783-66-6 |
| PubChem | 522683 |
| Número EINECS | 232-019-7 |
| ChemSpider | 455940 |
| SMILES |
|
| Propriedades | |
| Fórmula molecular | IF5 |
| Massa molar | 221.89 g/mol |
| Aparência | líquido amarelo pálido |
| Densidade | 3.250 g/cm3 |
| Ponto de fusão | 9.43 °C, 283 K, 49 °F |
| Ponto de ebulição | 97.85 °C, 371 K, 208 °F |
| Solubilidade em água | reage [1] |
| Estrutura | |
| Estrutura cristalina | monoclínico |
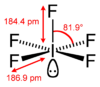
| Geometria de coordenação | quadrado piramidal |
| Forma molecular | quadrado piramidal[2] |
| Riscos associados | |
| MSDS | MSDS Externo |
| Principais riscos associados | tóxico, oxidante, corrosivo |
| NFPA 704 |  0 4 1 |
| Compostos relacionados | |
| Outros aniões/ânions | Pentóxido de iodo |
| Outros catiões/cátions | Pentafluoreto de bromo |
| Compostos relacionados | Monofluoreto de iodo Trifluoreto de iodo Heptafluoreto de iodo |
| Página de dados suplementares | |
| Estrutura e propriedades | n, εr, etc. |
| Dados termodinâmicos | Phase behaviour Solid, liquid, gas |
| Dados espectrais | UV, IV, RMN, EM |
| Exceto onde denotado, os dados referem-se a materiais sob condições normais de temperatura e pressão Referências e avisos gerais sobre esta caixa. Alerta sobre risco à saúde. | |
Pentafluoreto de iodo é um composto interhalogênico com a fórmula química IF5. Foi primeiramente sintetizado por Henri Moissan em 1891 pela queima de iodo sólido em gás fluor.[3] Essa reação química exotérmica ainda é usada atualmente para produzir IF5, embora as condições de reação tenham sido aprimoradas.[4][5]
Química
Ele reage vigorosamente com água formando ácido fluorídrico
e também reage com flúor gasoso, formando-se heptafluoreto de iodo.[4]
Aminas primárias reagem com pentafluoreto de iodo formando nitrilas após hidrólise.[6]
Toxicidade
O pentafluoreto de iodo produz uma grande quantidade de gases tóxicos quando derramado na água.[7]
Referências
- ↑ Patnaik, P. (2002). Handbook of Inorganic Chemicals. [S.l.]: McGraw-Hill. ISBN 0-07-049439-8
- ↑ Durbank, R. D.; Jones, G. R. (1974). «Crystal structure of Iodine Pentafluoride at -80° ». Inorganic Chemistry. 13 (5): 421–439. doi:10.1021/ic50135a012 !CS1 manut: Nomes múltiplos: lista de autores (link)
- ↑ Moissan, M. H. (1891). «Nouvelles Recherches sur le Fluor». Annales de Chimie et de Physique. 6 (24): 224–282
- ↑ a b Ruff, O.; Keim, R. (1930). «Das Jod-7-fluorid [The iodine-7-fluoride]». Zeitschrift für Anorganische und Allgemeine Chemie (em German). 193 (1): 176–186. doi:10.1002/zaac.19301930117 !CS1 manut: Língua não reconhecida (link)
- ↑ Ruff O.; Keim R. (1931). «Fluorierung von Verbindungen des Kohlenstoffs (Benzol und Tetrachlormethan mit Jod-5-fluorid, sowie Tetrachlormethan mit Fluor) [Fluoridation of Carbon Compounds (Benzene and Tetrachlormethane with Iodine-5-Fluoride, and Tetrachloromethane with Fluorine)]». Zeitschrift für Anorganische und Allgemeine Chemie (em German). 201 (1): 245–258. doi:10.1002/zaac.19312010122 !CS1 manut: Língua não reconhecida (link)
- ↑ Stevens, T. E. (1966). «Rearrangement of Amides with Iodine Pentafluoride». Journal of Organic Chemistry. 31 (6): 2025–2026. doi:10.1021/jo01344a539
- ↑ Associação Portuguesa de Segurança. «Manual de Intervenção em Emergências com Matérias Perigosas» (PDF). p. 292
 | Este artigo sobre um composto inorgânico é um esboço. Você pode ajudar a Wikipédia expandindo-o. |













