Tétrahydropyrane
| Tétrahydropyrane | |||
 | |||
| Structure du tétrahydropyrane | |||
| Identification | |||
|---|---|---|---|
| Nom UICPA | oxane | ||
| Synonymes | THP, 2H-tétrahydropyrane, oxacyclohexane, oxyde de pentaméthylène | ||
| No CAS | 142-68-7 | ||
| No ECHA | 100.005.048 | ||
| No CE | 205-552-8 | ||
| DrugBank | DB02412 | ||
| PubChem | 8894 | ||
| ChEBI | 46941 | ||
| SMILES | C1CCOCC1 PubChem, vue 3D | ||
| InChI | Std. InChI : vue 3D InChI=1S/C5H10O/c1-2-4-6-5-3-1/h1-5H2 Std. InChIKey : DHXVGJBLRPWPCS-UHFFFAOYSA-N | ||
| Propriétés chimiques | |||
| Formule | C5H10O [Isomères] | ||
| Masse molaire[1] | 86,132 3 ± 0,005 g/mol C 69,72 %, H 11,7 %, O 18,58 %, | ||
| Propriétés physiques | |||
| T° fusion | −49,2 °C[2] | ||
| T° ébullition | 88 °C[2] | ||
| Solubilité | 80 g·L-1[2] à 20 °C | ||
| Masse volumique | 0,88 g·cm-3[2] à 20 °C | ||
| Point d’éclair | −20 °C[2] ; −16 °C[3] | ||
| Pression de vapeur saturante | 9,53 kPa[2] à 25 °C | ||
| Précautions | |||
| SGH[2],[3] | |||
  Danger H225 : Liquide et vapeurs très inflammables H315 : Provoque une irritation cutanée H319 : Provoque une sévère irritation des yeux H335 : Peut irriter les voies respiratoires EUH019 : Peut former des peroxydes explosifs P210 : Tenir à l’écart de la chaleur/des étincelles/des flammes nues/des surfaces chaudes. — Ne pas fumer. P261 : Éviter de respirer les poussières/fumées/gaz/brouillards/vapeurs/aérosols. P305+P351+P338 : En cas de contact avec les yeux : rincer avec précaution à l’eau pendant plusieurs minutes. Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer. | |||
| Transport[2],[3] | |||
Code Kemler : 33 : matière liquide très inflammable (point d'éclair inférieur à 23 °C) Numéro ONU : 3271 : ÉTHERS, N.S.A. Classe : 3 Étiquette :  3 : Liquides inflammables Emballage : Groupe d'emballage II : matières moyennement dangereuses ; | |||
| Composés apparentés | |||
| Autres composés | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
Le tétrahydropyrane (THP), est un éther cyclique de formule brute C5H10O. C'est le plus simple des oxanes, constitué d'un cycle à six atomes dont un d'oxygène et cinq de carbone. Il s'agit d'un liquide incolore volatil inflammable. On rencontre plus fréquemment ses dérivés, les éthers de tétrahydropyranyle (THP-) étant des intermédiaires courants en synthèse organique par réaction d'alcools sur du dihydropyrane. Le cycle du tétrahydropyrane est notamment présent dans tous les oses en configuration pyranose, par exemple dans le glucopyranose. En phase gazeuse, il se présente en conformation chaise de symétrie Cs[4].
Préparation
L'hydrogénation du dihydropyrane au nickel de Raney est un mode de synthèse organique classique du tétrahydropyrane[5].
Utilisation
Le groupe 2-tétrahydropyranyle est utilisé comme groupe protecteur de groupes alcool lors de synthèses organiques[6],[7]. La réaction d'un alcool avec le dihydropyrane forme un cétal, un α-éther de tétrahydropyranyle, qui protège le groupe alcool d'un grand nombre de réactions :
-
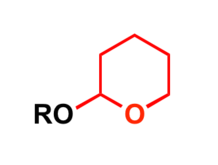 Éther de THP.
Éther de THP.
L'alcool peut être rétabli ultérieurement par hydrolyse acide avec formation de 5-hydroxypentanal.
-
 Groupe protecteur au THP en synthèse organique.
Groupe protecteur au THP en synthèse organique.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ a b c d e f g et h Entrée dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 8 juillet 2016 (JavaScript nécessaire)
- ↑ a b et c Fiche Sigma-Aldrich du composé Tétrahydropyrane anhydre, 99 %, consultée le 31 mars 2022.
- ↑ (en) J. D. Builth-Williams, S. M. Bellm, L. Chiari, P. A. Thorn, D. B. Jones, H. Chaluvadi, D. H. Madison, C. G. Ning, B. Lohmann, G. B. da Silva et M. J. Brunger, « A dynamical (e,2e) investigation of the structurally related cyclic ethers tetrahydrofuran, tetrahydropyran, and 1,4-dioxane », Journal of Chemical Physics, vol. 139, no 3, , p. 034306 (PMID 23883026, DOI 10.1063/1.4813237, lire en ligne)
- ↑ (en) D. W. Andrus, John R. Johnson, Nathan L. Drake et Charles M. Eaker, « Tetrahydropyran », Organic Syntheses, vol. 23, , p. 90 (DOI 10.15227/orgsyn.023.0090, lire en ligne)
- ↑ (en) R. A. Earl, L. B. Townsend, G. Saucy et G. Weber, « Methyl 4-hydroxy-2-butynoate », Organic Syntheses, vol. 60, , p. 81 (DOI 10.15227/orgsyn.060.0081, lire en ligne)
- ↑ (en) Arthur F. Kluge, A. Pilli, Kenneth S. Kirshenbaum, Clayton H. Heathcock et K. Barry Sharpless, « Diethyl[(2-tetrahydropyranyloxy)methyl]phosphonate », Organic Syntheses, vol. 64, , p. 80 (DOI 10.15227/orgsyn.064.0080, lire en ligne)
 Portail de la chimie
Portail de la chimie















