Nitrure de calcium
| Nitrure de calcium | |||
 | |||
| Identification | |||
|---|---|---|---|
| No CAS | 12013-82-0 | ||
| No ECHA | 100.031.435 | ||
| No CE | 234-592-9 | ||
| PubChem | 3387080 | ||
| Apparence | solide cristallin rouge/brun | ||
| Propriétés chimiques | |||
| Formule | Ca3N2 [Isomères] | ||
| Masse molaire[1] | 148,247 ± 0,012 g/mol Ca 81,1 %, N 18,9 %, | ||
| Propriétés physiques | |||
| T° fusion | 1 195 °C | ||
| Masse volumique | 2,63 g·cm-3 à 25 °C[2] | ||
| Cristallographie | |||
| Système cristallin | cubique | ||
| Symbole de Pearson | |||
| Classe cristalline ou groupe d’espace | Ia-3 (no 206) cubique Hermann-Mauguin : | ||
| Précautions | |||
| SGH[2] | |||
 H260 : Dégage, au contact de l'eau, des gaz inflammables qui peuvent s'enflammer spontanément H314 : Provoque de graves brûlures de la peau et des lésions oculaires P223 : Éviter tout contact avec l’eau, à cause du risque de réaction violente et d’inflammation spontanée. P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage. P231+P232 : Manipuler sous gaz inerte. Protéger de l’humidité. P305+P351+P338 : En cas de contact avec les yeux : rincer avec précaution à l’eau pendant plusieurs minutes. Enlever les lentilles de contact si la victime en porte et si elles peuvent être facilement enlevées. Continuer à rincer. P370+P378 : En cas d’incendie : utiliser … pour l’extinction. P422 : Stocker le contenu sous … | |||
| Transport[2] | |||
Numéro ONU : 3208 : MATIÈRE MÉTALLIQUE HYDRORÉACTIVE, N.S.A. Classe : 4.3 Étiquette :  4.3 : Matières qui, au contact de l'eau, dégagent des gaz inflammables | |||
| Unités du SI et CNTP, sauf indication contraire. | |||
modifier  | |||
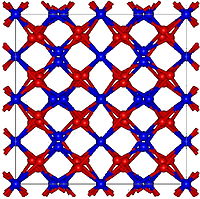
Le nitrure de calcium est un solide cristallin rouge/brun composé de calcium et d'azote. Il possède une structure anti-bixbyite comme le Mn2O3 sauf que la position des ions est inversée, ainsi la calcium prend la position du manganèse et l'azote celle de l'oxygène.
Le nitrure de calcium peut être produit directement à partir des corps simples correspondant aux atomes qui le constituent :
- 3 Ca + N2 → Ca3N2
Il peut réagir avec l'humidité de l'air, ou directement avec l'eau pour donner de l'ammoniac et de la chaux (éteinte) :
- Ca3N2 + 6 H2O → 3 Ca(OH)2 + 2 NH3
Au-dessus de 350 °C il réagit aussi avec le dihydrogène :
- Ca3N2 + 2 H2 → 2 CaNH + CaH2
Notes et références
v · m | |
|---|---|
|
v · m | |
|---|---|
 Portail de la chimie
Portail de la chimie
















