Chloramphénicol acétyltransférase

Pour les articles homonymes, voir CAT.
Chloramphénicol O-acétyltransférase
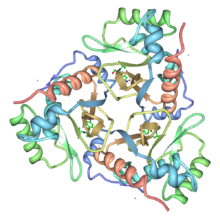
Structure d'une CAT de type III (PDB 3CLA[1])
| N° EC | EC 2.3.1.28 |
|---|---|
| N° CAS | 9040-07-7 |
| IUBMB | Entrée IUBMB |
|---|---|
| IntEnz | Vue IntEnz |
| BRENDA | Entrée BRENDA |
| KEGG | Entrée KEGG |
| MetaCyc | Voie métabolique |
| PRIAM | Profil |
| PDB | RCSB PDB PDBe PDBj PDBsum |
| GO | AmiGO / EGO |
modifier 
La chloramphénicol acétyltransférase (CAT) est une acétyltransférase qui catalyse la réaction :
- acétyl-CoA + chloramphénicol CoA + acétate de chloramphénicol.
Cette enzyme, présente chez certaines bactéries[2], intervient dans la détoxication du chloramphénicol, conférant à ces bactéries une résistance à cet antibiotique[3]. Cette réaction d'acétylation, dans laquelle un résidu d'histidine de l'extrémité C-terminale joue un rôle déterminant, empêche le chloramphénicol de se lier aux ribosomes.
Notes et références
- ↑ (en) A.G.W. Leslie, « Refined crystal structure of type III chloramphenicol acetyltransferase at 1·75 Å resolution », Journal of Molecular Biology, vol. 213, no 1, , p. 167-186 (PMID 2187098, DOI 10.1016/S0022-2836(05)80129-9, lire en ligne)
- ↑ (en) J. Engel et D. J. Prockop, « The Zipper-Like Folding of Collagen Triple Helices and the Effects of Mutations that Disrupt the Zipper », Annual Review of Biophysics and Biophysical Chemistry, vol. 20, , p. 137-152 (PMID 1867713, DOI 10.1146/annurev.bb.20.060191.001033, lire en ligne)
- ↑ (en) W. V. Shaw, L. C. Packman, B. D. Burleigh, A. Dell, H. R. Morris et B. S. Hartley, « Primary structure of a chloramphenicol acetyltransferase specified by R plasmids », Nature, vol. 282, no 5741, , p. 870-872 (PMID 390404, DOI 10.1038/282870a0, lire en ligne)
v · m | |
|---|---|
| 2.3.1 : groupes autres que aminoacyle (principalement acétyltransférases) |
|
| 2.3.2 : aminoacyltransférases |
|
| 2.3.3 : groupe converti en alkyle pendant le transfert |
|
 Portail de la biochimie
Portail de la biochimie  Portail de la biologie cellulaire et moléculaire
Portail de la biologie cellulaire et moléculaire










